Tekst: Anu Planken
Fotod: Aivar Kullamaa
Regionaalhaigla onkoloogia-hematoloogia kliinikus on kliiniline ja siirdemeditsiiniline teadustöö hästi juurdunud ning onkoloogidel on suur huvi teadus-arendustöö vastu. Käsitlen järgnevalt mõnda käimasolevat teadusprojekti.
Dr Anu Planken, onkoloog ja vanemteadur
Pärast Tartu Ülikooli arstiteaduskonna lõpetamist oli mul sügavam huvi neuroloogia vastu. Kuna olin juba üliõpilasena tegelenud teadustööga neurofüsioloogia laboris, tundus loogiline jätkata õpinguid doktorantuuris neurobioloogia valdkonnas Helsingi Ülikooli biotehnoloogia instituudis prof Mart Saarma juhendamisel.
Minu teadustöö keskendus Parkinsoni tõve molekulaarsete protsesside iseloomustamisele ning uudsete haigust modifitseerivate ravimite väljatöötamisele. Tegemist oli peamiselt prekliinilise laboratoorse tööga ning aastal 2012 kaitsesin doktoritöö „Role of GDNF and its cross-talk with other growth-factors in the dopaminergic system“.
Pärast kaitsmist pöördusin tagasi Eestisse ning asusin tööle Vähiuuringute Tehnoloogia Arenduskeskuses (VTAK) kliiniliste uuringute juhina. Kuna VTAK-is olid käimas siirdemeditsiinilised uuringud koostöös onkoloogidega Regionaalhaiglast, tekkis mul sügavam huvi onkoloogia valdkonna vastu – sel erialal on muutused äärmiselt kiired ning minu teadustööl võib olla reaalne väljund kasvajate diagnostikas ja ravis. Tegelesin aktiivselt ka teadustööga onkoloogia residentuuri vältel ning alates 2019. aasta sügisest jätkan karjääri arst-teadlasena, pühendudes pool ajast kliinilisele tööle onkoloogina ning teise poole ajast akadeemilisele ja teadus-arendustööle vanemteadurina Tartu Ülikoolis ja biotehnoloogia ettevõttes Icosagen.
1. NEUROTROOFSETE TEGURITE ROLL NÄRVISÜSTEEMI JA KASVAJA VAHELISTES INTERAKTSIOONIDES
Lähtuvalt oma teadustaustast olen soovinud integreerida aastatepikkust kogemust neurobioloogias onkoloogia valdkonnaga ning minu jaoks kõige inspireerivam uuring käsitleb kasvajate ja närvisüsteemi vahelisi seoseid.
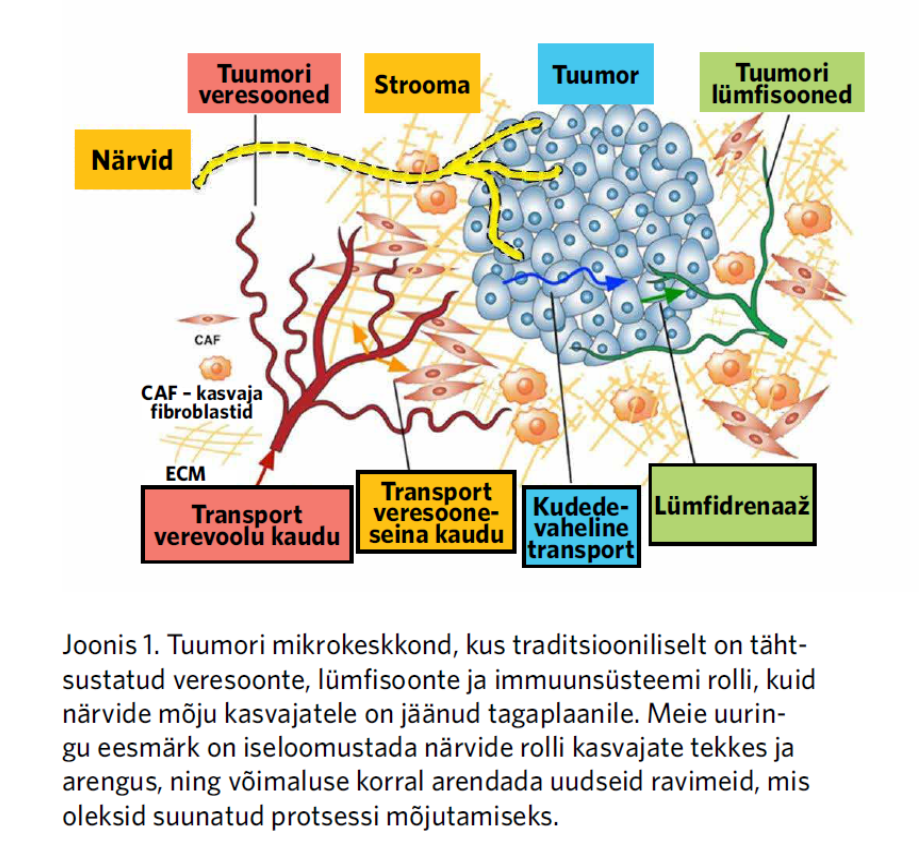
Kasvajate molekulaarsed mehhanismid on komplekssed ning paljusid bioloogilisi protsesse peetakse keskseteks kasvajate patogeneesis (nn hallmarks of cancer). Viimasel ajal on kasvajate bioloogias hakatud tähtsustama tuumori mikrokeskkonna mõju kasvajate arengule, kuna lisaks kasvajarakkudele esinevad kasvajakoes ka strooma komponendid, nagu veresooned, närvid ja immuunsüsteemi rakud, mis interakteerudes mõjutavad kasvajarakkude paljunemist ja levikut. Mikrokeskkonna mõjust lähtuvalt on teostatud ulatuslikult uuringuid, mõistmaks angiogeneesi ja immuunregulatsiooni rolli kasvajates. Tänapäeva onkoloogias on kliinilises praktikas kasutusel mitu sihtmärklaudravimit nimetatud protsesside modifitseerimiseks, kuid puuduvad põhjalikud uuringud, mis käsitleksid närvisüsteemi rolli kasvajate tekkes ja arengus, ning puuduvad ravimid, mis oleksid suunatud selliste protsesside mõjutamise vastu (vt ka joonis 1).
Närvisüsteemi rolli kasvajate arengus tuntakse küll juba aastast 1940, kui publitseeriti esimesed tööd, mis näitasid, et kasvajate denervatsioonil on kasvajavastane efekt. Vaatamata sellele on vähe uuringuid, mis käsitleksid molekulaarseid mehhanisme, mis mõjutavad kasvaja- ja närvisüsteemi vahelisi interaktsioone. Sellest kontekstist lähtuvalt on välja pakutud, et vähirakud mõjutavad otseselt närve ja indutseerivad innervatsiooni läbi neuriitide väljakasvu tuumori suunas (protsess, mida tuntakse kui neo-neurogenees) ning samal ajal sekreteerivad neuronid ja gliiarakud tuumori kasvu, invasiooni ja migratsiooni stimuleerivaid molekule, mis soodustavad kasvaja levikut mööda närve (protsess, mida tuntakse kui perineuraalne invasioon, PNI). Histoloogias loetakse kasvajaid PNI positiivseteks, kui 33% närvist on ümbritsetud kasvajarakkude poolt, ning aina enam hakatakse tähtsustama seda markerit kui halva prognoosi näitajat enamiku levinud kasvajate puhul, nagu pea-kaela-, pankrease-, kolorektaal-, rinna- ja prostatakasvajad.
Neurotroofsed faktorid (NTF) on sekreteeritavad biomolekulid, mida tuntakse närvisüsteemi arengu ja homöostaasi faktoritena, kuid esmased tulemused viitavad asjaolule, et neil faktoreil võib olla ka keskne roll kasvajate neurobioloogias. On publitseeritud esmaseid uuringuid, kus on käsitletud klassikaliste neurotroofsete faktorite rolli kasvajates, näiteks on näidatud, et nii pankrease-, rinna- kui ka sapiteedekasvajad üleekspresseerivad neurotroofseid faktoreid ning nimetatud valkudel on kemoatraktiivne mõju kasvajarakkudele. Lisaks on leitud, et nimetatud faktorite türosiinkinaasi retseptorite (n.RET, MET, NTRK) mutatsioonidel on keskne roll eri kasvajate nn „driver“-mutatsioonidena. Lisaks eespool loetletud klassikalistele kasvufaktoritele iseloomustati 15 aastat tagasi kolme uudset neurotroofset faktorit: kasvu diferentseerumise faktor 15 (GDF15), mesentsephaalsetest astrotsüütidest pärinev neurotroofne faktor (MANF) ja tserebraalne dopamiini neurotroofne faktor (CDNF). Need uudsed neurotroofsed faktorid on neuroloogilisest aspektist relevantsed, kuna hoiavad elus keskaju dopamiini neuroneid ja käituvad neuroprotektiivselt Parkinsoni tõve mudelites, kuid meie esmased uuringud on näidanud, et neil võib olla roll ka kasvajate proliferatsioonis, metastaseerumises ja ravimresistentsuse tekkes ning lisaks ka kasvajatest indutseeritud anoreksia ja kahheksia puhul.
Selleks, et uurida neurotroofsete faktorite rolli kasvajate puhul, oleme käivitanud põhjaliku uuringu koostöös Regionaalhaigla onkoloogia kliiniku, patoloogiakeskuse ning Tallinna Tehnikaülikooli ja Tartu Ülikooli teadlastega. Eesmärk on esimest korda iseloomustada neurotroofsete faktorite võimalikku esinemist ja rolli inimeste kasvajatel. Selle siirdemeditsiinilise uuringu eesmärk on selgitada, kas ja kuidas need faktorid mõjutavad kasvajate teket ja arengut ning kas faktorite mõjutamisel võiks olla kasvajavastane terapeutiline väljund. Kasutades rahvusvahelistest geeniekspressiooni andmebaasidest saadud infot, oleme määranud bioinformaatilise analüüsi abil erinevate neurotroofsete faktorite tasemed tuhandetest kasvajaproovidest eri kasvajatüüpide puhul. Lisaks oleme teinud geeni ekspressiooni mõõtmisi Regionaalhaiglas kogutud 200 kolorektaal-, rinnakasvaja ja melanoomiproovidest ning hetkel käib põhjalik immunohistokeemiline analüüs nende faktorite valgutasemete iseloomustamiseks kasvajakudedes. Uuringut juhivad Regionaalhaigla patoloog dr Katrin Lepik ja laborispetsialist Birgit Truumees. Lisaks profileerime ka melanoomi ja kolorektaalkasvajate seerumeid neurotroofsete faktorite tasemete suhtes ning uuringu põhjal on Tallinna Tehnikaülikooli magistrandil Kristel Ratasel plaanis kaitsta 2020. aasta suvel oma magistritöö. Esmased tulemused toetavad meie hüpoteesi, et neurotroofsetel teguritel on oma roll kasvajate patogeneesis, ning see annab aluse edasisteks uuringuteks ja võimalike uudsete ravimite arendamiseks.
2. UUTE VÄHIVASTASTE BIOLOOGILISTE RAVIMITE ARENDAMINE
Teine suuremahuline uuring keskendub uudsete vähivastaste bioloogiliste ravimkandidaatide arendamisele. Uuring toimub koostöös Regionaalhaigla, Tartu Ülikooli tehnoloogia instituudi ning biotehnoloogia ettevõttega ICOSAGEN. Uuringu sisuks on uudsete onkoloogiliste ravimkandidaatide selekteerimine, bioloogiliste antikehade tootmine ja valideerimine prekliinilistel loomamudelitel.
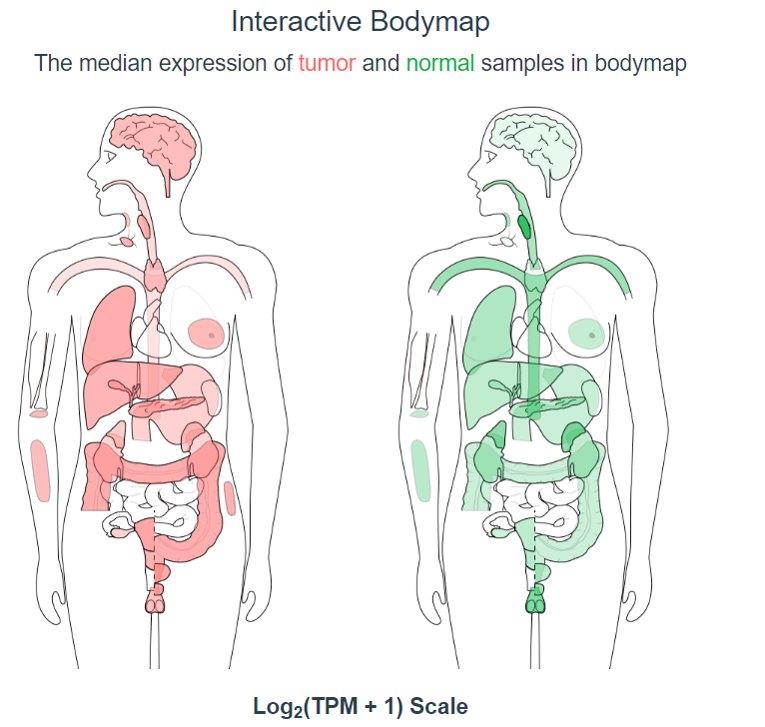
Joonis 2. Mesentsephaalsetest astrotsüütidest pärineva neurotroofse faktori geeni ekspressioonitasemete võrdlus erinevate vähipaikmete puhul (märgitud punasega) ning normaalkudedes (märgitud rohelisega).
Projekti esimeses faasis oleme teinud põhjaliku bioinformaatilise analüüsi, kasutades vähirakuliinide genoomi editeerimise tehnoloogia (CRISPR-Cas9) süsteemil põhinevaid andmeid, mille põhjal oleme koostanud vähivastaste sihtmärkide nimekirja (179 membraanvalku). Uuringu eesmärk on arendada nimetatud valguliste sihtmärkide vastu antagonistlikke bioloogilisi ravimeid. Kasutades Tartu Ülikooli teadlaste väljatöötatud ja optimeeritud antikehade tootmise tehnoloogiaid (Hybrifree, VLP), oleme alustanud bioloogiliste ravimite lähtemolekulide (kimäärsete antikehade) arendamisega. Selleks oleme määratlenud vähivormid, mille vastu antikehapõhist bioloogilist ravi on võimalik ja vajalik arendada (kaasa arvatud pankrease-, soole-, rinna- ja kopsuvähk), ning selekteerinud sihtmärkmolekulid, mis on ekspresseeritud rakupinnal.
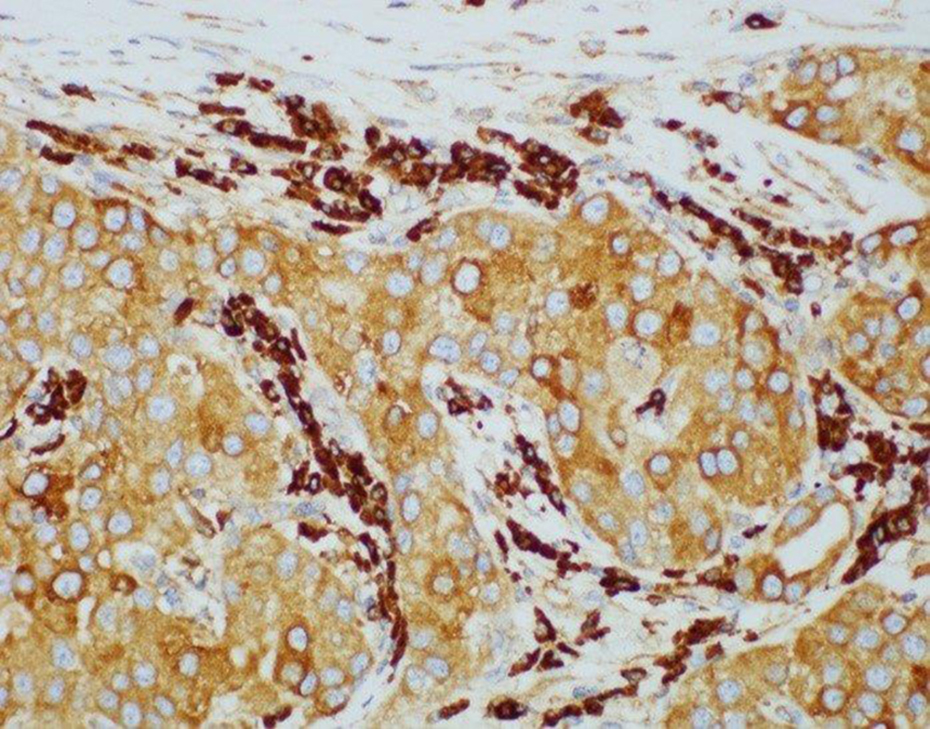
Joonis 3. Mesentsephaalsetest astrotsüütidest pärineva neurotroofse faktori valgu eskpressioon rinnakasvaja kudedes.
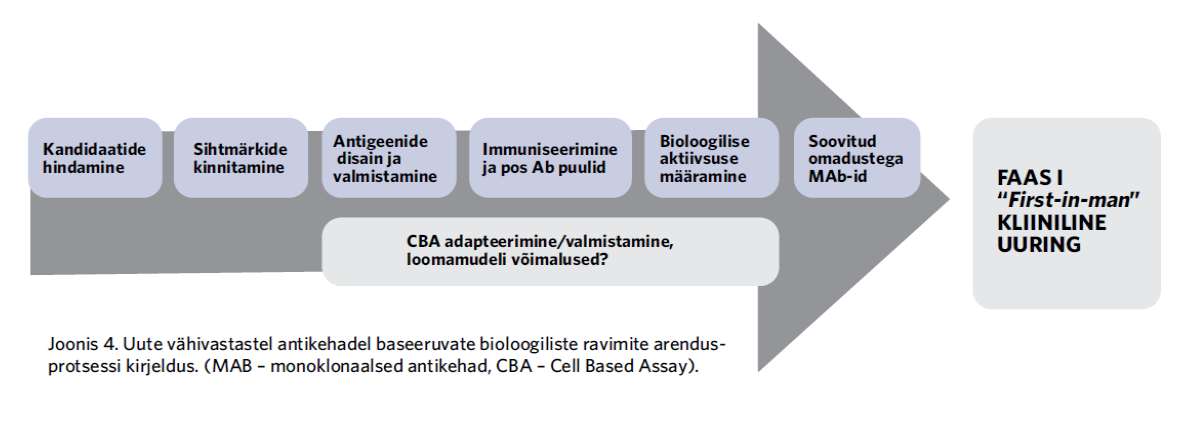
Hetkel käib antikehade tootmine ning kanade-küülikute immuniseerimise etapp. Arendatud molekulide puhul verifitseerime esmalt nende soovitava bioloogilise aktiivsuse ja testime in vitro ning in vivo kasvajate loomamudelites. Võimaluse korral plaanime esimest korda Eestis ka sobivate kandidaatidega edasiarendusi faas I (first-in-man) kliiniliste uuringute tasemeni ning plaanime nende läbiviimist Regionaalhaiglas.
3. RAHVUSVAHELISED KOOSTÖÖPROJEKTID
Onkoloogia kliinikus on käimas ka rahvusvahelisi uuringuid, neist olulisimad on koostööprojektid EORTC-ga (European Organisation for Research and Treatment of Cancer), mis on üks peamisi akadeemilisi ja kliinilisi uuringuid tegevaid organisatsioone onkoloogia valdkonnas Euroopas. EORTC SPECTA projektiga on juba eelnevalt kopsuvähi valdkonnas liitunud dr Kersti Oselin ning käimas on ulatuslik metastaatilise kopsuvähiga patsientide kasvajakudede molekulaarse profileerimise uuring. Alates 2020. aastast on meil võimalus liituda nii SPECTA kui ka lisauuringuga – IMMUCAN, kolorektaalvähi kasvajate kontekstis. Uuringu eesmärk on üleeuroopaline platvorm, kuhu kogutakse eri kasvajapaigetega patsientide kliinilised, diagnostilised ja kasvajate DNA sekveneerimise andmed, mida saavad kõik EORTC liikmed kasutada ka isiklikuks teadustööks. IMMUCAN-i uuringu raames lisandub uuringule ka immuunprofileerimine, et saada lisainformatsiooni tuumori immunobioloogiast ja mikrokeskkonnast.
EORTC grupist lähtunud konsortsiumiga andsime äsja sisse ka Marie Skłodowska-Curie Innovative Training Networksi (ITN) taotluse, mis keskendub maokasvajate raviresistentsuse tekkemehhanismide uurimisele ja uudsete ravivõimaluste väljatöötamisele. Projekti raames on eesmärk kaasata ka rahvusvahelisi doktorante ning koostöös Tartu Ülikooli arstiteaduskonnaga on plaanis ka Eestis koolitada nelja aasta jooksul üks välisdoktorant.

Onkoloog dr Anu Planken, patoloog dr Katrin Lepik ja laborispetsialist Birgit Truumees peavad teadusest lugu.
