Kasvaja genoomi profileerimine vereproovist ehk vedeliku biopsia võimaldab tuvastada raviks olulisi sihtmärkgeene, ennustada ravitulemust ning diagnoosida haiguse progressiooni isegi kuid varem kui kliinilised ja radioloogilised uuringud. Veres ringlev kasvaja rakuvaba DNA ehk ctDNA (ingl cell-free tumor DNA) on uus paljulubav meetod vähiravi personaalsemaks muutmisel, selgus ajakirjas Personalized Cancer Therapy ilmunud artiklist.
Milliseid uusi võimalusi loob vedeliku biopsia kasutamine?
Tavapärasel biopsiameetodil on mitmeid piiranguid. Sageli on asukoha tõttu kasvajamaterjali raske kätte saada ja seda eriti kordusbiopsiate korral. Lisaks võib biopsia sageli sisaldada diagnoosimiseks liiga vähe kasvajamaterjali või kasvajakoe heterogeensuse tõttu anda valenegatiivseid tulemusi. Patsientidelt, kes saavad hüübimisvastast ravi, on biopsiat võtta sootuks keeruline. Sellistel juhtudel on abiks üha enam kasutust leidev vedeliku biopsia, kus kasvajast lähtuvaid mutatsioone hinnatakse veres ringleva kasvaja rakuvaba DNA (ctDNA) abil.
Teadusuuringud näitavad, et ctDNA on hea meetod, mis võimaldab tuvastada sihtmärkravi kandidaatgeene, ennustada ravivastust, avastada haiguse levimist enne kliinilist või radioloogilist leidu ning hinnata tekkinud ravimresistentsust ja kasvaja geneetilist heterogeensust. Meetodi laialdaseks kasutuselevõtuks on oluline tagada uuringute piisav tundlikkus, et tuvastada ka varastes staadiumites vähkkasvajate juhud. See eeldab laboritelt vajalike kvaliteedikontrollisüsteemide juurutamist ning laboritöötajate kõrget kvalifikatsiooni.
Individuaalse vähiravi määramiseks kogutakse erinevaid andmeid (vt joonis) – kliinilisi, ravi-, labori- ja biopsiaandmeid ning teavet ravi jälgimise ja piltdiagnostika kohta. Vedeliku biopsia on uus andmeallikas lisaks juba olemasolevatele. Kõigi nende andmete kokkupanek on hädavajalik, et tagada tõeliselt individuaalne vähiravi. Suur katsumus on luua digitaalsed platvormid nende kogutud andmete kiiremaks ja tõhusamaks analüüsimiseks.
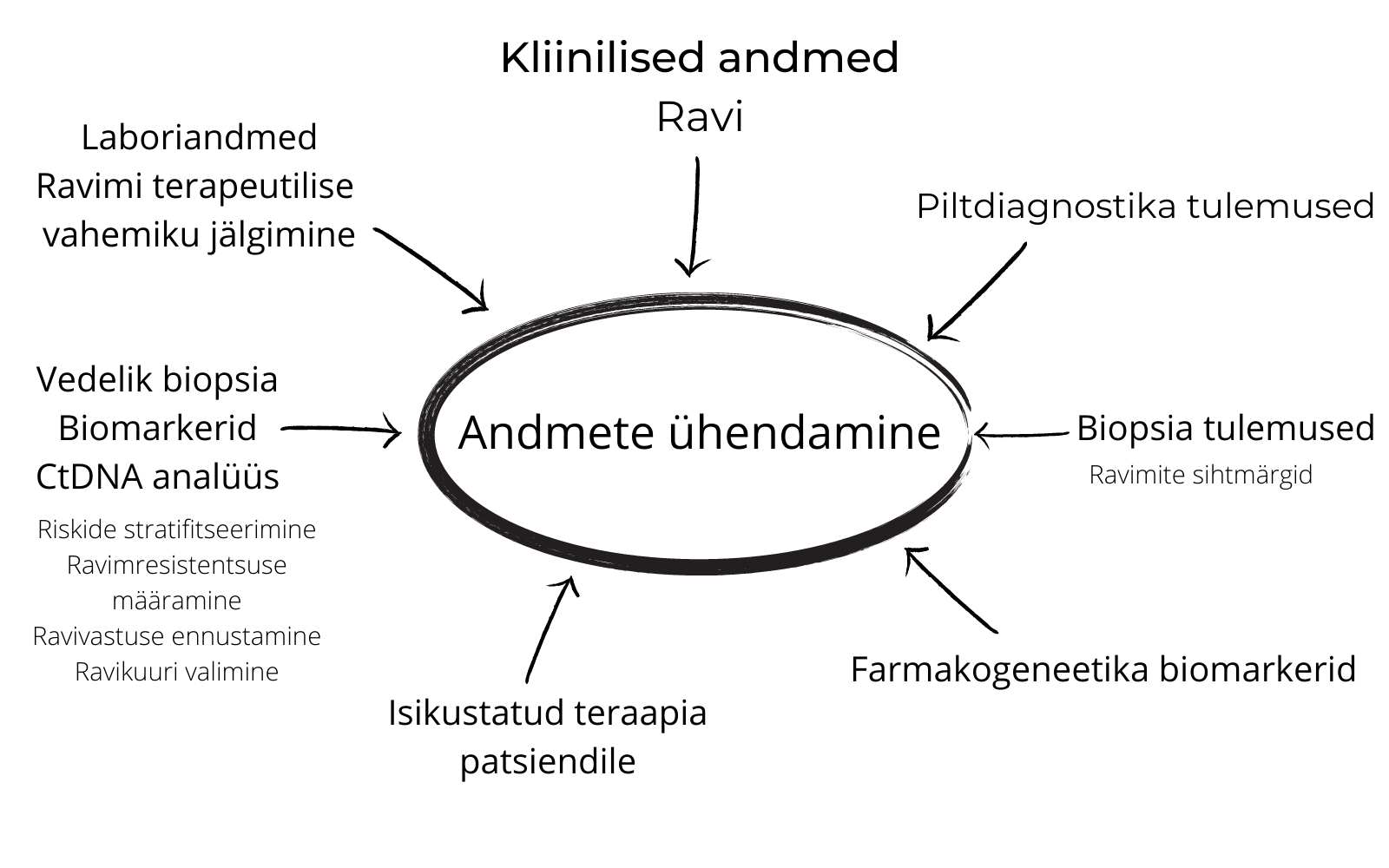
Joonis. Personaliseeritud vähiravi komponendid. Kohandatud Oellerich et al. 2019.
Mis on kasvaja rakuvaba DNA ja kuidas seda vähiravis kasutada saab?
Kasvaja genoom võib haiguse arenedes muutuda, seda eriti agressiivsemate vähivormide korral. Selliseid vähirakus tekkinud muutusi nimetatakse vähi somaatilisteks mutatsioonideks. Kui muutus on kaasasündinud ehk päritud vanematelt, nimetatakse seda iduliini mutatsiooniks ja sel juhul esineb muutus kõikides keharakkudes. Kasvajaraku lagunemisel vabaneb vereringesse kasvaja rakuvaba DNA (ctDNA), mille analüüsimine võimaldab määrata kasvaja geneetilist profiili ja selle järgi valida patsiendile sobivaim raviskeem. CtDNA analüüs võimaldab ravi ajal jälgida haiguse kulgu, ennustada ravivastust ja tuvastada haiguse progressiooni juba enne radioloogilist uuringut või kliinilisi sümptomeid. Proovivõtmise lihtsuse tõttu on verest teostatav vedeliku biopsia hea meetod pikaajalise ravi jälgimiseks.
Kasvaja rakuvaba DNA puhul uuritakse peamiselt kahte tüüpi muutuseid:
- kromosoomide ebastabiilsust. Vähirakkude paljunemisel tekivad vead, mis põhjustavad kromosoomide arvu erinevust rakkudes ehk aneuploidsust. Sellist nähtust nimetatakse kromosoomide ebastabiilsuseks (ingl chromosome instability CNI). Viimasest tulenevat kromosoomide koopia arvu ebastabiilsuse ehk CNI (ingl copy number instability) skoori on kasutatud näiteks eesnäärmevähi patsientidel pahaloomulise kasvaja eristamiseks ja ravivastuse ennustamiseks mitmete metastaatiliste kasvajate korral (nt mitteväikerakuline kopsuvähk, mitte-Hodgkini lümfoom jne). CNI vähenemine ravieelse tasemega võrreldes (vähenemine enam kui poole võrra) ennustas positiivset ravivastust või haiguse stabiliseerumist ja seda piltdiagnostika uuringust 3–8 nädalat varem;
- kasvajaga seotud mutatsioone või DNA metülatsiooni. CtDNA hüpermetülatsiooni määramist on rakendatud näiteks kolorektaalvähi diagnostikas ja taastekke hindamisel.
Somaatiliste mutatsioonide tõttu kasvaja rakus võib kujuneda välja ravimresistentsus. Näiteks mitteväikerakulise kopsuvähi puhul, kui EGFR (ingl epidermal growth factor receptor) geenis on mutatsioonid, mis aktiveerivad türosiinkinaasi tootmist ja põhjustavad seeläbi vähki, on võimalik sellist kasvajat ravida türosiini inhibiitoritega (nt gefitiniib). Kui vähikoes on tekkinud mutatsioon, mille puhul ravim ei saa enam seonduda EGFR geenilt toodetud retseptorile ja ei saa seetõttu takistada türosiinkinaasi tootmist, tekib patsiendil gefitiniibi suhtes ravimresistentsus. Seejärel saab jätkata ravi teise ravimiga. CtDNA uuring võimaldab vereproovist hinnata selliste mutatsioonide ja resistentsuse teket.
Ravi määramisel on oluline analüüsida ka iduliini muutuseid. Näiteks tiopuriin metüültransferaasi ensüümi puudulikkusega inimestel on oht merkaptopuriini (leukeemia ravim) toksikoosiks, kuna ravimi aeglase metabolismi tõttu kuhjuvad ravimi aktiivkomponendid organismi ja põhjustavad kõrvaltoimeid.
CtDNA analüüsimiseks kasutatakse erinevaid diagnostilisi platvorme, näiteks järgmise põlvkonna geenipaneelide, kogu genoomi ja kogu eksoomi sekveneerimise, reaalaja polümeraasi ahelreaktsiooni (ingl real-time PCR), digitaalse tilga polümeraasi ahelreaktsiooni (ingl digital droplet PCR) jt meetodeid. CtDNA määramisel tuleb arvestada ka teatud piirangutega, näiteks arvatakse, et ctDNA ei ole määratav mõne vähipaikme asukoha ja suuruse korral ja piiranguid võib seada ka uuringumeetod. Seetõttu soovitatakse praegu sageli ctDNA uuringut teha koos tavapäraste meetoditega (kasvaja biopsia proovist teostatavad uuringud).
Rohkem näited ctDNA kasutusvõimalustest vähiravis saab lugeda originaalartikli täistekstist.
Hinnang rakuvaba DNA kasutamise võimalikkusele onkoloogias
Kasvaja genoomi profileerimine vereproovist ehk vedeliku biopsia võimaldab tuvastada vähiraviks vajalikke sihtmärkgeene, ennustada ravitulemust ning diagnoosida haiguse progressiooni oluliselt varem kui kliinilised ja radioloogilised uuringud seda igapäevases kliinilises praktikas võimaldavad.
Vedeliku biopsia on oluline, kuna tavapärasel biopsiameetodil on mitmeid piiranguid. Sageli on probleemiks kasvajamaterjali piiratud kättesaadavus (nt kasvaja asukoha tõttu) ja umbes pooltel juhtudel saadakse biopsia diagnoosimiseks liiga vähe kasvajamaterjali või osutub proovi vastus kasvajakoe heterogeensuse tõttu valenegatiivseks. Hüübimisvastast ravi saavatelt patsientidelt on biopsiat võtta eriti keeruline, sest selleks tuleb antikoagulantide tarvitamine ajutiselt katkestada.
Veres ringlev kasvaja DNA (ctDNA) on kasvajast lähtuv fragmenteeritud DNA, mis ei ole seotud rakkudega. CtDNA analüüsimisel on võimalik kindlaks määrata kasvaja geneetiline profiil ja selle järgi valida patsiendile parim võimalik personaalne raviskeem. Ravi ajal võimaldab ctDNA analüüs jälgida haiguse kulgu (nt et vajaduse korral muuta raviskeemi), ennustada ravivastust ja tuvastada haiguse progressiooni enne kliiniliste haigussümptomite või radioloogiliste muutuste teket.
Maailmas kasutatakse palju erinevaid vedeliku biopsial põhinevaid vähigenoomi testide paneele, mis uurivad sadu vähiga seotud geene. Uuringul on võimalik tuvastada nii uusi kui ka juba teadaolevaid geenimuutusi, sealhulgas asendusmutatsioone, insertsioone või deletsioone, koopiaarvu muutusi ja geeni ümberkorraldusi. On võimalik hinnata ka vähi cfDNA osakaalu (ingl tumor fraction).
Eesti vähikeskustes kasutatakse kõige sagedamini FoundationOne Liquid CDx vähigenoomi testi soliidtuumoritega patsientidele. See test uurib ja annab tagasisidet kuni 300 vähiga seotud geeni kohta. Kliiniliselt keerukatel juhtudel, kui näiteks haiguse algkolle on ebaselge või patsiendi standardravi võimalused ammendunud, on testi tulemustele toetuvast individualiseeritud raviplaanist olnud sageli palju abi. Kuna praegu Eesti Haigekassa kahjuks testi maksumust veel ei kompenseeri, siis uuringu kompensatsioon põhineb haige omaosalusel.
Tulevikus võiks vedeliku biopsiast olla palju abi ka vähi personaliseeritud sõeluuringute või varase avastamise programmide kujundamisel, sest spetsiaalseid kasvajapaneele kasutades peaks vereanalüüsi põhjal saama vähiriski ning preinvasiivset ja varast invasiivset vähki oluliselt varem diagnoosida, kui kaasaegsed radioloogilised ja endoskoopilised uuringud seda võimaldavad. Samuti võimaldab vähiriski täpne ja õigeaegne teadmine teha muutusi tervisekäitumises ja kasutada teisi vähi teket ennetavaid meetmeid.
Vahur Valvere, Põhja-Eesti Regionaalhaigla onkoloogia ja hematoloogiakliiniku onkoloog-ülemarst ja Eesti Vähiliidu nõukogu esimees
Artikkel on ilmunud 25.02.21 Tervise Arengu Instituudi kodulehel: https://www.tai.ee/et/tegevused/personaalmeditsiin/uudiskiri/5017-rakuvaba-dna-muudab-vaehiravi-personaalsemaks?fbclid=IwAR0rNmPC_RdERhHghoxJdjSh34Bfp-YOYAH-mqnErEqgkZdWO9MtCe55W5g.
